活動概要
紀伊半島の神経風土病-筋萎縮性側索硬化症・パーキンソン・認知症複合(Kii ALS/PDC)
紀伊半島南部の牟婁(むろ)地方には、進行性の筋萎縮症、パーキンソン病に似た動作緩慢と筋強直、意欲低下が目立つ認知症の3症状出現を特徴とする神経風土病があり、筋萎縮性側索硬化症(ALS)・パーキンソンン認知症複合 (PDC)と呼ばれる。多発地名にちなんで牟婁病と呼ばれることもある。脳には、神経細胞とグリア細胞の中に、細胞骨格形成に関与するタウ蛋白のリン酸化産物が、異常蛋白として大量に蓄積する。グアム南部地域のチャモロ人にも類似疾患が多発する。近年、ALSの激減と並行してPDCの増加が確認され、生活習慣の変化と高齢化が病気の姿を変化させた可能性が考えられている。病気を起こす原因として、遺伝素因に何らかの環境要因が働いて多発や減少を引き起こした可能性があり、多面的に原因研究が進められている。
三重大学名誉教授 葛原茂樹
トピックス
過去のトピックス一覧- 牟婁病 徒然草 Vol.3
古座川と穂原の違い
紀伊半島には、和歌山県の古座川と三重県の穂原という二つの集積地がある。
紀伊半島南部は、明治以降、ALSの多発地として知られていた。1960年代に和歌山医大の疫学調査によって2ヵ所の多発地が発見された。1) 後で述べるように、古座川はALSの患者がほとんどだったため、和歌山医大の調査もALSに焦点が当てられた。そのため後年、“紀伊半島はALSの多発地”、という印象が持たれることになった。一方、穂原では、1960年代の調査でも ALSとともにPDCと考えられる患者が存在していた。1) ただ、和歌山医大の調査が古座川を中心に行われたこともあり、ながらくPDCは注目されなかった。
1990年代になって、我々は穂原地区で初めてのPDC剖検例を報告し、紀伊半島にPDCが実在することを証明した。2) 我々のこれまでの調査研究で、古座川はALSの多発地であったがPDCはほとんど存在しないこと、家族歴がなく大部分が孤発性であること、脳内のタウ蛋白はごく少量であること、一部の患者で C9orf72遺伝子変異3)またはOPTN遺伝子変異4)を認めること、がわかった。一方、穂原では、ALSとPDCの両者が存在すること、70%以上が家族性であること、脳内には多量のタウ蛋白の蓄積を認めること、C9orf72遺伝子変異やOPTN遺伝子変異例は認めないこと、(図1) などグアムALS/PDCと酷似していることがわかった。
グアムではALS/PDCが2000年代にはほぼ消滅したのに対して、穂原地区では依然として新規患者がみられている。(図2) ALS/PDCの発症には、環境要因が大きな役割を果たしているが、グアムで無くなり穂原で残っている環境因子の同定がこの疾患の謎を解く鍵である。
- Essay of Muro disease Vol.2
ALS/PDC and Cycads (2)
BMAA, a toxin derived from cycads
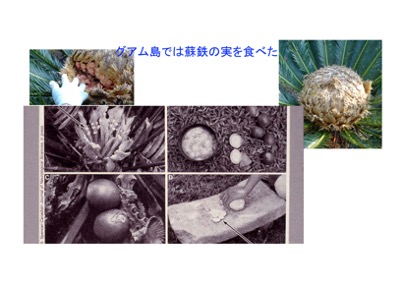
Cycads (Cycad) are toxic in themselves, and if eaten, they must be repeatedly soaked in water to remove the toxins, otherwise they can cause acute liver damage and, in the worst case, death. In Guam, people once ground the seeds of cycads that had been soaked in water, made a paste, and baked it into a tortilla-like bread. This was a high-calorie starch-based food. (Figure 1)
The acute toxicity of cycads is caused by formaldehyde, which is produced when cycasin is metabolized. Formaldehyde is also a carcinogenic substance. The cycad theory in Guam was proposed by Leonard T. Kurland (1921-2001), a leading expert in neuroepidemiology at the U.S. National Institutes of Health (NIH), based on field research conducted by cultural anthropologist M. Whitnee. It was later continued by Peter Spencer and Paul A. Cox.
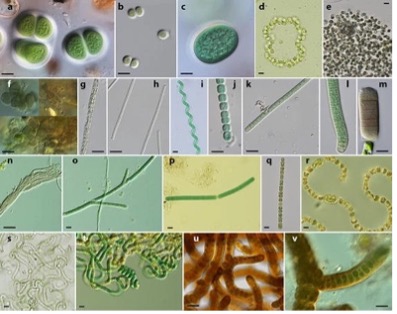
BMAA (β-methylamino-L-alanine), which is suspected to be a cause of ALS/PDC, is a non-protein amino acid produced by cyanobacteria (blue-green algae) (Figure 2) that parasitize the roots of cycad. Cyanobacteria have existed on Earth since ancient times and produce oxygen from carbon dioxide. The Chamorro people of Guam had a tradition of eating fruit bats. Paul A. Cox hypothesized that BMAA was concentrated in the fruit bats that ate cycad fruits, and that consuming these bats led to the onset of ALS/PDC in the Chamorro people (Figure 3). We therefore analyzed BMAA levels in the brains of ALS/PDC patients from Kii using mass spectrometry. The results showed that BMAA was not detected1).
On the other hand, Peter Spencer proposed that MAM (methylazoxymethanol), a compound generated during the conversion of cycathin to formaldehyde, is the true neurotoxin. Additionally, he explained that in the Kii Peninsula, where cycad are not consumed, the disease may develop from taking a traditional Chinese medicine made by boiling the seeds of cycad2). However, while traditional Chinese medicines derived from cycad do exist, they are not used in the affected areas, and this explanation feels somewhat forced.
1) Kokubo Y, Banack SA, Morimoto S, Murayama S, Togashi T, Metcalf JS, Cox PA, Kuzuhara S. β-N-methylamino-L-alanine analysis in the brains of patients with Kii ALS/PDC. Neurology 2017;89:1091-1092.
2) Spencer PS, Ohta M, Palmer VS. Cycad use and motor neurone disease in Kii peninsula of Japan. Lancet 1987;2:1462-1463
- 牟婁病 徒然草 Vol.2

お知らせ
過去のお知らせ一覧- Kii ALS/PDC 診療マニュアル
「紀伊半島南部に多発するALSとALS-parkinsonism-dementia complex に関する診療マニュアル」日本神経学会に承認され、掲載されました。
Kii ALS/PDC患者様の診療にお役立てください。
【日本神経学会承認ガイドラインウェブページ】
- 過去病理標本の研究使用について (2015年4月4日)
ご遺族の皆様へ
私たちの研究グループは、三重県内に多発する神経難病である「紀伊半島の筋萎縮症、パーキンソン症候群、認知症」について、長年診療及び研究を行っております。これまでに、多くの患者様及びご遺族のご意思により、本疾患の原因や発病メカニズムを明らかにし、新しい治療法を見つけるために病理解剖を行なわせて頂き、本疾患に関する数多くの新しい発見があり、それをもとに新しい治療法を見いだすことに尽力して参りました。しかしながら、未だ本疾患の根本的な原因は判明しておりません。
今回、研究をさらに発展させて病気の原因を明らかにするために、これまで三重県内の病院や施設において2000年ころまでに病理解剖にご協力頂きました神経難病の患者様の病理標本について、新しい方法で再検討させて頂きたいと考えております。対象となられる患者様の病理検体は、病気の解明に不可欠であると考えております。
しかしながら、亡くなられてからすでに数十年が経過しており、改めてご遺族から本研究に対するご同意を得ることが極めて困難な状況にあります。そこで、三重大学医学部倫理委員会に申請し、ご遺族の同意に代えて当該研究ホームページ上に標本の研究利用を一定期間公知することで研究同意に代えさせて頂くということで承認されました。
ご遺族の皆様におかれましては、本疾患の原因を明らかにし、治療法や予防法を確立するために、ご理解とご協力を賜りますよう、何卒宜しくお願い申し上げます。ご質問などございましたら、ホームページ記載のご連絡先に宜しくお願い申し上げます。- Kii ALS/PDCの「診断基準」および「重症度分類」の策定
スケジュール
過去のスケジュール一覧- 臨床神経病理検討会(Web CPC)
2020年6月27日(土)
臨床神経病理検討会(Web CPC)を予定しています。
- 環境医学研究所 市民公開講座 2017 「神経難病の克服に向けて」
日時: 2017年10月21日(土) 13:00〜16:30
場所: 名古屋大学 東山キャンパス 野依記念学術交流館
講師: 山中宏二(環境医学研究所 教授)、岡野栄之(慶応義塾大学 教授)、小久保康昌(三重大学大学院 招聘教授)、饗場郁子(国立病院機構東名古屋病院 神経内科 リハビリテーション部長)
URL: 案内パンフレット- 第27回臨床神経病理検討会
2017年2月12日(日)
第27回臨床神経病理検討会を予定しています。